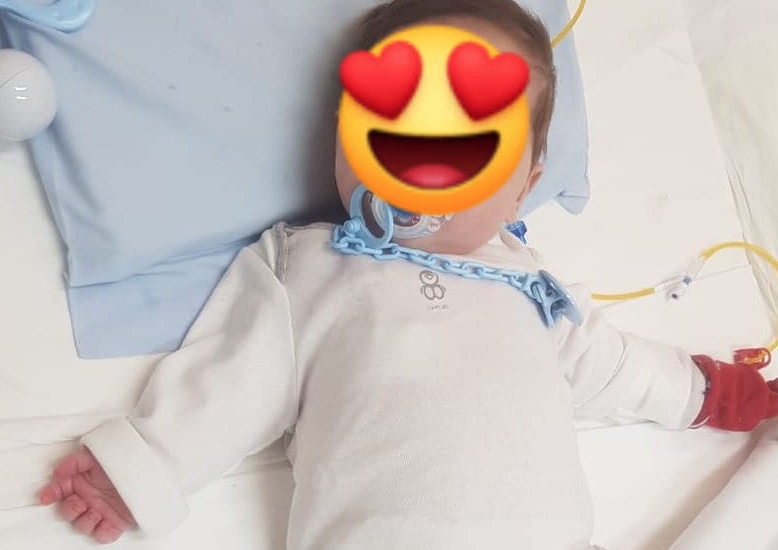
Il bambino affetto da linfoistiocitosi e ricoverato presso il Santobono Pausilipon. Fondamentale trovare un donatore di midollo osseo
Questa è una storia triste ma che potrebbe avere un finale straordinario. È la vicenda di Vincenzino che a soli 5 mesi già lotta per la vita. La sua piccola esistenza è stata colpita da una grave e non comune malattia: la linfoistiocitosi. Si tratta di una particolare sindrome che può essere sconfitta attraverso il trapianto di midollo osseo. Per questo è scattata la gara di solidarietà per aiutare il piccolo.
Tutto ha avuto inizio su Facebook dove è stata creata una pagina ad hoc. Poi è stato lanciato l’appello per trovare un donatore. E la risposta di Napoli e dei napoletani non si è fatta attendere. Tantissimi i messaggi di affetto per Vincenzino e di solidarietà per la sua famiglia. Molte le disponibilità da parte di numerose persone a rilasciare un proprio campione di saliva.
LA STORIA DI VINCENZINO E IL POST SU FACEBOOK – Ciao mi chiamo Vincenzino e sono nato il 4 ottobre 2019 , da quando ero nella pancia della mia mamma dicevano che avevo un problema all’intestino le anta intestinale dilatate poi quando sono nato sembrava che questo problema era scomparso , dopo vari accertamenti torno a casa con la mia mammina ma dopo qualche giorno che stavo a casa ho iniziato a vomitare e a fare diarrea così sono stato portato in ospedale dove mi hanno ricoverato e dopo fatto gastroscopia, colonscopia, tac,risonanza ecc ecc dicono alla mia mamma che devo nutrirmi con una sacca e che non posso ne bere ne mangiare finché non capiranno cosa ho di preciso passano giorni settimane mesi e i medici ancora devono capire cosa ho! Cosi dicono alla mamma che può portarmi a casa ma devo continuare a nutrirmi con questa sacca .A natale finalmente a casa ,ma non passa nemmeno qualche giorno che inizio ad avere la febbre altissima mi riportano all’ospedale dove mi fanno svariati esami (un altra batosta per la.mia mamma) suo figlio ha la LINFOISTOCITOSI e molto grave deve fare le chemio il 14 gennaio inizio le chemio che mi fanno stare tanto male ho appena 3 mesi e mezzo e peso poco più di 5 kl oggi 29 febbraio sto ancora al posolipon per le chemio da quando sono nato la.mia casa l’ho vista per pochi giorni…… voglio andare a casa con la mia mammina ma per farlo ho bisogno di un TRAPIANTO DI MIDOLLO OSSEO nella banca dove tengono i donatori nessuno è compatibile per me …..AIUTATEMI A TORNARE A VIVERE ….. se troverò il donatore dovrò affrontare anche l’intervento per l’intestino ruotato così dopo potrò mangiare come altri bambini …..sai io non conosco il sapore del latte! Non ho mai assaggiato niente non posso farlo ma se tu mi aiuti tu che leggi magari sei compatibile e puoi donarmi un po del tuo midollo……grazie cuore buono
LE ADESIONI – Volevo ringraziare tutti in nemmeno 24 ore abbiamo superato le 2300 persone ora spero che domani mattina il posilipon sia invaso di telefonate e di persone che voglio regalarmi un po del loro midollo 2000 grazie cuori buoni❤❤
LA MALATTIA (DAL SITO DELL’OSPEDALE BAMBIN GESÙ DI ROMA) –
CHE COS’È
La Linfoistiocitosi Emofagocitica primaria (HLH) è una malattia legata all’attivazione e alla proliferazione incontrollata di alcune cellule del sistema immunitario come i macrofagi, una classe di globuli bianchi che ha il compito di difendere il corpo dai microbi che possono causare malattie infettive.
Si riconoscono due forme di Linfoistiocitosi Emofagocitica:
– Una forma primitiva (Linfoistiocitosi Emofagocitica primaria o familiare);
– Una forma secondaria.
Distinguere le due forme è molto importante perché ha importanti conseguenze per la scelta della cura e per la prognosi.
Nella forma primitiva sono spesso documentabili una familiarità (ovvero più pazienti affetti nella stessa famiglia) e alterazioni genetiche specifiche. Tuttavia, nel 30% circa dei casi non è documentabile alcuna alterazione genetica. In quest’ultimo caso si devono quindi ricercare (ed escludere) le possibili cause di Linfoistiocitosi Emofagocitica secondaria.
Soltanto dopo aver escluso le cause di Linfoistiocitosi Emofagocitica secondaria si potrà porre la diagnosi di Linfoistiocitosi Emofagocitica primaria (diagnosi di esclusione).
Questa malattia colpisce circa 1 nuovo nato su 50.000 (quindi il numero di nuovi casi attesi in Italia è stimabile attorno a una decina l’anno). Il rapporto tra maschi e femmine è di circa 1:1.
QUALI SONO LE CAUSE
Dopo anni di ricerche sono stati identificati i difetti che causano la Linfoistiocitosi Emofagocitica Primitiva.
Si tratta della mancanza di alcune proteine essenziali per la funzione “killer” dei linfociti: nel 40% dei casi è in gioco un difetto della perforina, in un altro 30% dei casi un difetto di Munc13-4 e in casi più rari un difetto della Syntaxin 11. Più di recente è stata descritta una forma di Linfoistiocitosi Emofagocitica primaria associata ad una alterazione della Syntaxin Binding Protein 2 (STXBP2 o UNC18B).
Le mutazioni del gene della perforina determinano un deficit della proteina omonima. Questa viene secreta dai linfociti T citotossici e dalle cellule Natural Killer (NK) – grandi linfociti granulari in grado di uccidere le cellule bersaglio – in seguito al contatto tra queste cellule e il bersaglio.
La perforina è in grado di attraversare la membrana della cellula bersaglio dove forma dei pori che portano alla sua distruzione. Mutazioni nel gene codificante Munc 13-4 e Syntaxin 11 determinano un difetto nella fuoruscita dei granuli dalla cellula, quindi un difetto dei meccanismi con cui i T linfociti citotossici e le cellule NK danneggiano cellule bersaglio.
Tali difetti determinano una ridotta capacità (fino all’impossibilità) da parte del sistema immunitario di eliminare l’agente infettivo che ha innescato il processo infiammatorio e di autolimitare tale processo (come avviene normalmente). Tutto ciò crea un “circolo vizioso” che porta ad uno stato di eccessiva infiammazione che è caratteristico della malattia ed è responsabile dei sintomi della Linfoistiocitosi Emofagocitica primitiva.
La Linfoistiocitosi Emofagocitica primitiva è ereditata con modalità autosomico recessiva (ad eccezione di alcune varianti legate al cromosoma X): entrambi i geni, sia quello di origine materna che quello di origine paterna sono alterati nei bambini con Linfoistiocitosi Emofagocitica primitiva.
I genitori sono portatori di una copia alterata del gene (l’altra copia è normale) e non sono malati ma rischiano ad ogni gravidanza, con un 25% di probabilità, di avere un figlio malato.
Spesso i sintomi compaiono in seguito a un’infezione virale.
COME SI MANIFESTA
La Linfoistiocitosi Emofagocitica Primitiva si manifesta nel primo anno di vita nel 70% dei casi. Solo il 10% dei casi comincia a presentare sintomi nel periodo neonatale.
I sintomi più comuni sono rappresentati da:
– Febbre (spesso elevata);
– Ingrandimento progressivo di fegato e milza.
Meno frequentemente si presentano anche:
– Tumefazione dei linfonodi;
– Ittero (colorito giallastro della pelle e del bianco degli occhi);
– Eruzione cutanea maculo-papulare, vale a dire con lesioni cutanee sia piatte (macule) che in rilievo (papule).
Sintomi da riferire al sistema nervoso centrale, quali irritabilità, convulsioni, deficit dei nervi cranici, atassia (mancanza di coordinazione dei movimenti muscolari volontari), rigidità nucale e segni aspecifici di ipertensione endocranica, sono diagnosticati in circa un terzo dei pazienti.
Le alterazioni più comuni degli esami di laboratorio comprendono:
– Neutropenia e piastrinopenia (basso numero di granulociti neutrofili e di piastrine nel sangue);
– Concentrazioni elevate di ferritina, la proteina deputata al trasporto del ferro (uno dei reperti più suggestivi);
– Livelli elevati di trigliceridi (ipertrigliceridemia);
– Bassi livelli di fibrinogeno (ipofibrinoginemia);
– Ridotta attività funzionale in provetta delle cellule NK.
COME SI FA LA DIAGNOSI
Per definire la diagnosi sono stati sviluppati dei criteri internazionali. I criteri iniziali furono redatti nel 1991 e poi rivisti nel protocollo di trattamento HLH-2004.
Quest’ultimo prevede che la diagnosi possa essere formulata quando siano soddisfatti cinque dei seguenti otto criteri diagnostici iniziali:
Criteri clinici
– Febbre;
– Aumento di dimensioni della milza (splenomegalia).
Criteri di laboratorio
– Riduzione del numero di cellule del sangue (citopenia), che coinvolge almeno due linee cellulari;
– Ipertrigliceridemia e/o ipofibrinogenemia.
Criteri microscopici (istopatologici)
– Emofagocitosi (presenza di globuli rossi all’interno dei macrofagi) nel midollo osseo o nella milza o nei linfonodi.
Sono stati inoltre introdotti nuovi criteri diagnostici:
– Bassa o assente attività in provetta delle cellule NK;
– Ferritina superiore o uguale a 500 microgrammi/L;
– Aumentati livelli del recettore CD25 solubile (superiore a 2400 U/ml).
Con una storia familiare positiva, la diagnosi è definitiva (la consanguineità dei genitori rafforza la diagnosi). La diagnosi di Linfoistiocitosi Emofagocitica primitiva può anche essere basata sulla dimostrazione delle alterazioni genetiche sopra riportate.
COME SI CURA
In assenza di trattamento, la Linfoistiocitosi Emofagocitica Primitiva è rapidamente fatale con una sopravvivenza media di circa 2 mesi. È importante innanzitutto riconoscere la malattia e approntare tempestivamente non solo la terapia della stessa ma anche adeguate cure di supporto al paziente, soprattutto nelle fasi iniziali.
Ad esempio è importante curare le infezioni che “innescano” la comparsa dei sintomi della malattia. È pertanto indispensabile iniziare un trattamento in “mani esperte” prima che la malattia causi danni irreversibili o renda il trattamento meno efficace.
La sopravvivenza a 5 anni è del 10% nei casi trattati con polichemioterapia e di circa il 70% in quelli curati con trapianto di cellule staminali emopoietiche, che rappresenta l’unico trattamento in grado di guarire questa malattia.
I pazienti affetti da Linfoistiocitosi Emofagocitica primitiva, quindi con un difetto genetico che causa la malattia, possono essere curati soltanto quando il sistema immunitario che non funziona è sostituito con un sistema immunitario sano. È quello che accade quando il paziente viene sottoposto ad un trapianto di cellule staminali ematopoietiche. Tuttavia, prima di ricorrere al trapianto, è necessario ridurre lo stato di infiammazione incontrollata che è caratteristico della malattia.
Esistono raccomandazioni per la gestione della malattia e protocolli di terapia nazionali e internazionali. In particolare, i 2 protocolli maggiormente in uso sono l’HLH94 e l’HLH2004. Come prima linea di trattamento i bambini affetti possono essere trattati secondo gli schemi di terapia internazionali, con una combinazione di chemioterapia (etoposide, methotrexate), immunoterapia (siero anti-linfocitario, ciclosporina) e corticosteroidi. I pazienti con Linfoistiocitosi Emofagocitica Primitiva persistente o ricorrente in cui non è stato individuato nessun difetto genetico richiedono comunque un trapianto di cellule staminali ematopoietiche per la guarigione definitiva.
Per il trattamento della Linfoistiocitosi Emofagocitica Primitiva non vi sono farmaci approvati.
Di recente, è stato avviato, nel nostro Ospedale, un trial clinico con l’obiettivo di valutare l’efficacia e la sicurezza dell’impiego dell’anticorpo monoclonale ricombinante anti-interferone gamma (IFNɣ) nella terapia della Linfoistiocitosi Emofagocitica Primitiva.
I pazienti con Linfoistiocitosi Emofagocitica Primitiva hanno infatti alti livelli sierici di Interferone, proteina che causa l’infiammazione e il danno ai tessuti che si osserva nel corso della malattia. Neutralizzando l’Interferone, l’infiammazione potrà pertanto essere arrestata evitando il danno a carico degli organi e ripristinando le condizioni che permettono al piccolo paziente di procedere al trapianto che, come già sottolineato, è al momento l’unico strumento di cui disponiamo per guarire la Linfoistiocitosi Emofagocitica primitiva.